新型生物脫氮工藝中 N2O 產(chǎn)生及釋放研究進(jìn)展
王 賽,王淑瑩,鞏有奎,彭永臻,張靜蓉
(北京工業(yè)大學(xué)環(huán)境與能源工程學(xué)院,北京 100022)
摘 要:N2O 是重要的溫室氣體之一,微生物作用是大氣中 N2O 的主要產(chǎn)生源。大量污水脫氮工藝的研究及應(yīng)用表明,生物脫氮過程中 N2O 主要產(chǎn)生于微生物的硝化和反硝化代謝過程。近年來(lái),許多新型生物脫氮工藝已逐步應(yīng)用到實(shí)際污水處理中。本文闡述了硝化、反硝化階段 N2O 的產(chǎn)生機(jī)理,并分析了傳統(tǒng)生物脫氮工藝及同步硝化反硝化、短程硝化 - 反硝化、厭氧氨氧化、反硝化除磷等新型工藝中 N2O 的產(chǎn)生量及其影響因素,提出在追求高脫氮效率的同時(shí),優(yōu)化系統(tǒng)運(yùn)行條件及種群結(jié)構(gòu),可在一定程度上降低系統(tǒng) N2O 的產(chǎn)量及危害,為新型生物脫氮工藝實(shí)際運(yùn)行過程中降低N2O 的產(chǎn)量提供參考。
關(guān)鍵詞:N2O;產(chǎn)生機(jī)理;新型生物脫氮工藝
中圖分類號(hào):X703.1 文獻(xiàn)標(biāo)識(shí)碼:A 文章編號(hào):1000-3770(2010)03-0005-005
水體富營(yíng)養(yǎng)化是當(dāng)前全球重大的環(huán)境問題之一,生物脫氮除磷作為解決富營(yíng)養(yǎng)化的手段已成為污水處理領(lǐng)域的研究熱點(diǎn)。隨著研究工作的不斷深入,人們對(duì)脫氮除磷的微生物學(xué)機(jī)理有了新的認(rèn)識(shí), 開發(fā)了許多新型生物脫氮除磷工藝。在對(duì)新型脫氮工藝的研究中發(fā)現(xiàn),污水生物脫氮過程中氣態(tài)產(chǎn)物除N2 之外,還有 N2O 的積累與釋放。N2O 是一種強(qiáng)力的溫室氣體,等摩爾濃度 N2O 的增溫潛勢(shì)是 CO2 的 200~300 倍[1]。N2O 在大氣中不會(huì)下沉,不會(huì)被沖洗掉,其在對(duì)流層中很穩(wěn)定,且可不斷累積,停留時(shí)間長(zhǎng)達(dá) 120 年[2]。據(jù)報(bào)道,N2O 的大氣濃度每增加 1倍就將導(dǎo)致全球升溫 0.3℃[3]。研究表明,污水生物脫氮過程是N2O 的重要產(chǎn)生源。新型生物脫氮工藝能夠較為經(jīng)濟(jì)、有效地去除廢水中的氮污染物,但是在解決水環(huán)境問題的同時(shí),更應(yīng)盡量避免隨之產(chǎn)生的其它環(huán)境問題。因此,深入了解 N2O 在生物脫氮過程中的產(chǎn)生機(jī)制,以及不同生物脫氮工藝中 N2O 的釋放量有著極為重要的理論及實(shí)際意義。
1 生物脫氮過程中N2O 產(chǎn)生的微生物學(xué)機(jī)理
現(xiàn)有的大量研究表明,污水生物脫氮過程中微生物的硝化及反硝化代謝過程是污水處理中 N2O的主要產(chǎn)生源。
1.1 硝化過程
劉秀紅等[4]的研究發(fā)現(xiàn),硝化作用是生物脫氮中產(chǎn)生 N2O 的主要來(lái)源。生物硝化過程包括 2 個(gè)階段:第 1 個(gè)階段是氨氮在氨氧化菌(Ammonia-oxi- dizing bacteria,AOB) 的作用下氧化為亞硝酸鹽(NO -),羥胺(NH OH)是該反應(yīng)過程的中間產(chǎn)物,起 催 化 作用的酶有氨單加氧 酶(Ammonia mono-oxygenase,AMO) 和羥胺氧化還原酶(Hy- droxylamine oxidoreductase,HAO);第 2 個(gè)階段是經(jīng)亞硝酸鹽氧化 菌 (Nitrite-oxidizing bacteria, NOB)氧化為硝酸鹽(NO -),起催化作用的酶是亞硝酸氧化還原酶(Nitrite oxidoreductase,NOR)。
N2O 是作為硝化階段首過程的副產(chǎn)物出現(xiàn)的。在正常的硝化反應(yīng)階段,N2O 可能產(chǎn)生的途徑有 2 個(gè):(1) 亞硝酸鹽在 NOR 作用下的還原反應(yīng),即硝化菌的反硝化作用。當(dāng)溶解氧受限制時(shí),硝化反應(yīng)無(wú)法進(jìn)行徹底,導(dǎo)致亞硝酸鹽的積累,硝化菌利用氨氮氧化過程中提供的電子經(jīng)異化還原反應(yīng)將其轉(zhuǎn)化為 N2O 而釋放[5]。(2)亞硝酸鹽或氨氧化中間產(chǎn)物羥胺的化學(xué)分解作用[6]。
在硝化階段,除自養(yǎng)型硝化菌作用之外,許多異養(yǎng)微生物也可以進(jìn)行硝化作用。異養(yǎng)硝化菌的硝化速率是自養(yǎng)菌的 1/(100~1000)倍,而且只有在較高的有機(jī)物負(fù)荷(COD/N>10)和低 DO 下才能占優(yōu)勢(shì)起到硝化作用[7]。盡管如此,Anderson[8]的研究表明,在純菌種培養(yǎng)試驗(yàn)中,異養(yǎng)硝化菌 A aecalis 硝化過程產(chǎn)生的N2O 比自養(yǎng)菌 N europaea 產(chǎn)生的多。除此之外,好氧反硝化菌也可能產(chǎn)生 N2O,Inamori 等[9]認(rèn)為 A faecalis 能在好氧反硝化的過程中產(chǎn)生 N2O。
1.2 反硝化過程
反硝化是由異養(yǎng)型兼性厭氧微生物將硝酸鹽或亞硝酸鹽還原為氮?dú)獾倪^程。傳統(tǒng)的反硝化按照 4 個(gè)階段進(jìn)行,如圖 1 所示。

可以看出,N2O 是反硝化過程的中間產(chǎn)物。由于 NO 有劇毒,以NO 為產(chǎn)物的細(xì)菌難以生存,因此,產(chǎn)生的 NO 會(huì)快速轉(zhuǎn)化為 N2O[10]。在不同反應(yīng)條件下,N2O 和 N2 都有可能作為反硝化的最終產(chǎn)物釋放。能否控制并保持氧化亞氮還原酶(Nos)的活性是抑制N2O 產(chǎn)生的關(guān)鍵。研究發(fā)現(xiàn),系統(tǒng)中低 DO,亞硝酸鹽的積累,低 pH 等環(huán)境因素都會(huì)抑制 Nos 的活性而導(dǎo)致N2O 的積累與釋放[11-13]。除此之外,低 COD/N 比導(dǎo)致不完全反硝化也是產(chǎn)生 N2O 的重要原因。
在脫氮過程中,除了硝化和反硝化作用產(chǎn)生 N2O 外,還會(huì)發(fā)生異化性硝酸鹽還原作用(DNRA)。該過程中,亞硝酸鹽和硝酸鹽可用作電子受體還原成氨。該作用常發(fā)生在電子受體貧乏的缺氧環(huán)境中[14]。對(duì)該過程起催化作用的是硝酸鹽還原酶(Nar)和亞硝酸鹽還原酶(Nir)。Bleakley 等[15]在研究中發(fā)現(xiàn)異化性硝酸鹽還原作用能產(chǎn)生 N2O,硝酸鹽呼吸細(xì)菌的增長(zhǎng)十分迅速,是一類不屬于反硝化菌的產(chǎn) N2O 菌群。因此,生物脫氮過程中 N2O 的產(chǎn)生不僅僅局限于傳統(tǒng)脫氮過程,微生物的多樣性使得 N2O 的來(lái)源更多,產(chǎn)生機(jī)理更加復(fù)雜。
2 不同污水脫氮工藝中 N2O 的產(chǎn)生分析
全程硝化 - 反硝化工藝是目前污水處理廠應(yīng)用較多的生物脫氮工藝。近年來(lái),許多新型生物脫氮工藝:同步硝化 - 反硝化,短程硝化 - 反硝化及厭氧氨氧化等工藝的研究與開發(fā),使得經(jīng)濟(jì)高效地去除污水中的含氮污染物成為可能。但是,研究表明,在不降低脫氮效率的前提下,新型生物脫氮工藝可能會(huì)導(dǎo)致 N2O 產(chǎn)量的增加。因此,在關(guān)注這些新技術(shù)、新工藝脫氮效率的同時(shí),也應(yīng)該關(guān)注其排放產(chǎn)物對(duì)大氣環(huán)境的影響。
2.1 全程硝化 - 反硝化工藝
該工藝在好氧條件下, NH + 首先被 AOB 氧化成 NO - 再被 NOB 氧化成 NO -,在缺氧條件下,NO -被還原為 N2。
在硝化階段,DO 對(duì) N2O 的產(chǎn)生與釋放有重要的影響,高 DO 濃度有利于降低 N2O 產(chǎn)生量,當(dāng) DO 質(zhì)量濃度低于 0.9 mg·L-1 時(shí),將導(dǎo)致 N2O 產(chǎn)生量的迅速升高[16]。Galle Tallec 等[17]研究發(fā)現(xiàn)DO=1 mg·L-1時(shí),氧化亞氮產(chǎn)生率較高(7.1 μg·g-1SS·h-1)。低 DO導(dǎo)致 N2O 較高的原因是:AOB 在低 DO 下可能進(jìn)行反硝化作用。該過程中,NO - 取代氧作為電子受體。另外,氨氮對(duì) NOB 有抑制作用,若氨氮濃度過高,容易造成亞硝酸鹽的積累,使 N2O 產(chǎn)量增加[18]。這也是傳統(tǒng)脫氮工藝不適合處理高濃度氨氮廢水的原因。
反硝化過程中 C/N 比是系統(tǒng)中 N2O 產(chǎn)生的重要因素。Sunjin Hwang 在研究中發(fā)現(xiàn),當(dāng) C/N 比為 3 時(shí),好氧和缺氧反應(yīng)器中都沒有發(fā)現(xiàn) N2O 的釋放, 但當(dāng) C/N 比由 3 降低到 2 時(shí),缺氧系統(tǒng)中產(chǎn)生了質(zhì)量濃度為 130 mg·L-1 的 N2O [19]。原因可能是碳源不足,導(dǎo)致反硝化不徹底,N2O 成為反應(yīng)的產(chǎn)物。 Hanaki 等[13]指出當(dāng) C/N 比迅速下降時(shí),反硝化階段有大量的 N2O 釋放。Itokawa[20]的研究中,C/N 比低于 3.5,有 20%~30%的氮以 N2O 的形式排放。另外,系統(tǒng)中溶解氧的存在會(huì)導(dǎo)致 N2O 的產(chǎn)生[5]。
從實(shí)現(xiàn) N2O 減量化的角度出發(fā),在硝化階段應(yīng)保持較高的溶解氧,較低的氨氮負(fù)荷,以減少亞硝酸鹽的積累;反硝化階段避免溶解氧的存在,C/N 比應(yīng)大于 3.5。除此之外,較大的 SRT(> 10 d)和適當(dāng)?shù)膒H(6.8~8)也可以減少 N2O 的產(chǎn)生[5]。
2.2 同步硝化反硝化
同步硝化反硝化(Simultaneous nitrification and denitrification,SND)脫氮是在好氧狀態(tài)下硝化和反硝化在一個(gè)反應(yīng)器內(nèi)同時(shí)進(jìn)行的過程。關(guān)于同步硝化反硝化產(chǎn)生的機(jī)理,廣泛接受的解釋有以下 2 種:存在的條件下直接把氨氮轉(zhuǎn)化為氣態(tài)產(chǎn)物去除,許多異養(yǎng)硝化菌也能進(jìn)行好氧反硝化。因此,從微生物學(xué)角度來(lái)看同步硝化反硝化生物脫氮是可能的。
Zeng 等[25]在 SBR 系統(tǒng)中,控制 DO 質(zhì)量濃度在 0.5 mg·L-1,通過中間產(chǎn)物 NO - 的積累,成功實(shí)現(xiàn)了 SND,經(jīng)測(cè)定系統(tǒng)釋放的氣體大部分是 N2O 而不是 N2。Beline 等[26]在低氧條件下實(shí)現(xiàn)了同步硝化反硝化,用 15N 示蹤技術(shù)發(fā)現(xiàn)反硝化產(chǎn)生的 N2O 占總氮的 27%,是同步硝化反硝化 N2O 產(chǎn)生的主要過程。呂錫武運(yùn)用 SBR 反應(yīng)器,將同步硝化反硝化與傳統(tǒng)硝化反硝化工藝進(jìn)行了對(duì)比,在總氮去除率相差不大的前提下,同步硝化反硝化產(chǎn)生的 N2O 比傳統(tǒng)工藝少,后者是前者的 1.5 倍[27]。在實(shí)現(xiàn)同步硝化反硝化的運(yùn)行條件方面,C/N 比小于 4,DO 質(zhì)量濃度濃度大于 2 mg·L-1,都會(huì)增大 N2O 的產(chǎn)生量[28]。
2.3 短程硝化 - 反硝化工藝
短程硝化反硝化工藝是將硝化反應(yīng)控制在亞硝酸鹽階段,直接進(jìn)行反硝化反應(yīng)(見圖 2)。與全程脫氮相比,短程工藝能節(jié)省 25%的氧消耗量和 40% 的外碳源消耗量。但是,在對(duì) N2O 產(chǎn)生量的研究方面卻不容樂觀,這對(duì)在全球采用新工藝處理污水的形勢(shì)下提出了一個(gè)亟待解決的問題。
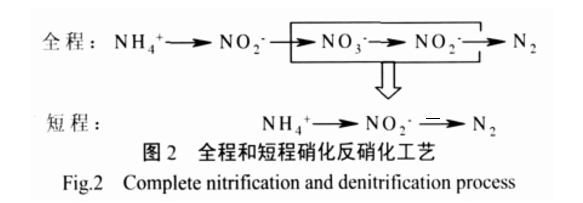
根據(jù)現(xiàn)有的研究結(jié)論可知,亞硝酸鹽的積累是短程硝化 - 反硝化階段 N2O 產(chǎn)生較多的主要原因。M J Kampschreur [21]認(rèn)為,短程硝化階段 N2O 產(chǎn)生的主要來(lái)源是 AOB 的反硝化作用。硝化過程中亞硝酸鹽的積累會(huì)導(dǎo)致 AOB 以亞硝酸鹽為電子受體進(jìn)行反硝化,導(dǎo)致 N2O 的積累與釋放。有報(bào)道稱,亞硝酸鹽的積累是反硝化過程產(chǎn)生 N2O 的重要原因,當(dāng)NO - 質(zhì)量濃度 ρ(N)=1 mg·L-1 時(shí)就會(huì)對(duì) N O 的還原產(chǎn)生抑制[13]。Lemaire R[22]也有類似的研究,抑制N2O 還原的 NO - 質(zhì)量濃度 ρ(N)=5 mg·L-1。但劉秀紅[4]發(fā)現(xiàn),短程脫氮過程中 N2O 主要產(chǎn)生在硝化階段,反硝化階段不但沒有 N2O 產(chǎn)生,硝化階段積累的溶解性 N2O 反而會(huì)進(jìn)一步還原為 N2。Yan Zhou [23]研究結(jié)果表明,反硝化中抑制 N2O 還原的是游離亞硝酸(Free nitrous oxide,F(xiàn)NA),而不是亞硝酸鹽。當(dāng) FNA 質(zhì)量濃度ρ(NO --N)=0.000 7~0.001 mg·L-1 時(shí),抑制作用為 50%;當(dāng) FNA 質(zhì)量濃度大于 0.004 mg·L-1時(shí),其對(duì)N2O 的還原完全抑制。有關(guān)于亞硝酸鹽對(duì)N2O 還原的抑制作用還需要進(jìn)一步的研究。
短程脫氮過程中,氨氮負(fù)荷的增加,水力停留時(shí)間(HRT)的減少,鹽度的增加,DO 的降低都會(huì)導(dǎo)致亞硝酸鹽的積累,是 N2O 產(chǎn)生的間接因素;而在短程反硝化階段,即使 C/N 比降到 0.5,也沒有發(fā)現(xiàn) N2O 的增加 [17],這說明 C/N 比并不是短程脫氮中N2O 積累的主要因素。
2.4 厭氧氨氧化工藝
研究發(fā)現(xiàn),氨的氧化可在無(wú)氧但存在硝酸鹽或亞硝酸鹽的情況下發(fā)生。以硝酸鹽或亞硝酸鹽為電子受體,氨作為直接電子供體,還原硝酸鹽或亞硝酸氮并將其轉(zhuǎn)化為氮?dú)獾姆磻?yīng)(見圖 3),稱為厭氧氨氧化(ANAMMOX)。
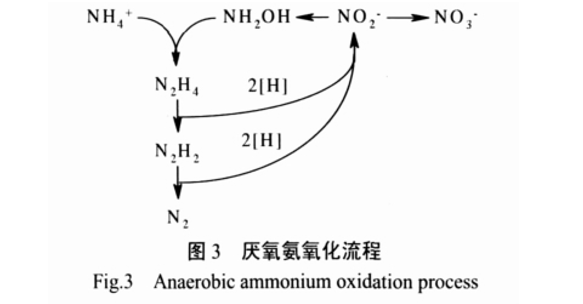
Voets 等運(yùn)用硝化- 厭氧氨氧化 2 個(gè)反應(yīng)器進(jìn)行研究,發(fā)現(xiàn)厭氧氨氧化反應(yīng)器中 N2O 占進(jìn)水總氮的0.6%,由于厭氧氨氧化菌沒有發(fā)現(xiàn)有產(chǎn)生 N2O 的生理功能,因此推測(cè)是硝化段中的氨氧化細(xì)菌進(jìn)入到厭氧氨氧化反應(yīng)器中發(fā)生反硝化的結(jié)果[29]。Kartal 等[30] 的研究證明厭氧氨氧化菌在還原硝態(tài)氮時(shí),并不經(jīng)過傳統(tǒng)的產(chǎn)生N2O 的反硝化過程。只有質(zhì)量分?jǐn)?shù) 0.26% 的氮以N2O 的形式釋放,對(duì)此合理的解釋是 N2O 來(lái)自NO 的去毒作用,NO 是厭氧氨氧化的中間產(chǎn)物;另一種可能是產(chǎn)生于羥胺的氧化還原作用。
與傳統(tǒng)的硝化 - 反硝化脫氮過程相比,短程硝化-ANAMMOX 脫氮過程可使運(yùn)行費(fèi)用減少90%,不產(chǎn)生 N2O 氣體,具有顯著地可持續(xù)性和高經(jīng)濟(jì)效益的特點(diǎn)[31]。因此,短程硝化-ANAMMOX 工
藝具有較高的開發(fā)價(jià)值和良好的應(yīng)用前景。
2.5 反硝化除磷工藝
反硝化除磷是利用反硝化除磷細(xì)菌 (DPB)以硝酸鹽代替氧作為電子受體將反硝化脫氮和生物除磷兩個(gè)原本彼此獨(dú)立的過程合二為一。反硝化除磷解決了城市污水 C/N 比較低的環(huán)境下反硝化與除磷競(jìng)爭(zhēng)有限碳源的矛盾,具有“一碳兩用”的優(yōu)勢(shì); 而缺氧代替好氧則節(jié)省了曝氣的能量消耗,同時(shí)減少了污泥產(chǎn)量。
系統(tǒng)中共同存在時(shí),大部分的反硝化是由反硝化聚糖菌完成的,當(dāng)NO - 質(zhì)量濃度ρ(N)高于1~2 mg·L-1 時(shí)會(huì)產(chǎn)生 NO -,原因可能是 NO - 的積累抑制了 N O還原酶的活性[32]。Lemaire[33]的研究也有類似的結(jié) 論,在反應(yīng)過程中,聚糖菌而不是聚磷菌進(jìn)行反硝化作用,并且釋放的氣體以 N2O 為主,在將反硝化聚磷的污泥和反硝化污泥混合并加入外碳源后,N2O的釋放量迅速減少。目前,對(duì)反硝化吸磷過程中產(chǎn)生氣體的分析比較少,對(duì)此工藝中 N2O 的產(chǎn)生還需進(jìn)一步的研究。
2.6 好氧脫氮工藝
好氧脫氮工藝是 1997 年首先由德國(guó) Hannover 大學(xué)提出的新型生物脫氮工藝[34]。在許多實(shí)際生物脫氮系統(tǒng)中,經(jīng)常會(huì)出現(xiàn)氨的超量去除,這種氨和硝酸鹽的超量去除現(xiàn)象稱為好氧脫氮。Muller[35]研究 發(fā)現(xiàn),好氧反硝化速率與氨消耗速率基本處于同一數(shù)量級(jí),這使好氧反硝化更具有實(shí)際的工程意義。其發(fā)生地可能條件有以下幾點(diǎn):(1) 一些硝化細(xì)菌除了能夠進(jìn)行正常的硝化作用外,還能進(jìn)行反硝化作用。(2)一些反硝化細(xì)菌除了能在無(wú)氧條件下進(jìn)行正常的反硝化作用外,還能在有氧條件下進(jìn)行反硝化作用(即當(dāng)氧受限制時(shí),同時(shí)以氧和硝酸鹽作為電子受體)。(3)還有一些細(xì)菌能彼此合作,進(jìn)行序列反應(yīng),把氨轉(zhuǎn)化為氮?dú)鈁36]。
雖然好氧反硝化工藝可在 DO 較高的條件下進(jìn)行 ,但 N2O 釋放量遠(yuǎn)高于低 DO 條件下 N2O 的釋放量[37]。Inamori 等[9]認(rèn)為好氧反硝化菌在好氧條件下還原硝酸鹽生成的 N2O 比在缺氧條件下多得多,但是也有報(bào)道稱純好氧反硝化菌株的產(chǎn) N2O 量低于傳統(tǒng)反硝化菌[38]。目前好氧反硝化菌對(duì) N O 的貢獻(xiàn)還沒有統(tǒng)一的定論。

3 結(jié) 論
微生物的硝化和反硝化是污水脫氮過程中產(chǎn)生N2O 的 2 個(gè)主要階段。其產(chǎn)生機(jī)理并沒有統(tǒng)一的結(jié)論。基于傳統(tǒng)脫氮工藝?yán)碚摶A(chǔ)上開發(fā)的各種新型脫氮工藝已逐漸運(yùn)用于實(shí)際污水處理中。研究發(fā)現(xiàn), 新型的脫氮工藝雖然在脫氮效率,運(yùn)行費(fèi)用上較傳統(tǒng)工藝占優(yōu)勢(shì),但在溫室氣體 N2O 產(chǎn)生方面卻不容樂觀。因此,研究及實(shí)際應(yīng)用過程中應(yīng)避免走進(jìn)一味追求高脫氮效率的誤區(qū)。
在生物脫氮的過程中,運(yùn)行條件和微生物群落對(duì)N2O 的產(chǎn)量起到關(guān)鍵性的作用。N2O 的減量化應(yīng)該從這兩個(gè)方面進(jìn)行。通過優(yōu)化系統(tǒng)運(yùn)行條件,可有效降低生物脫氮過程中 N2O 的釋放量;同時(shí),優(yōu)化微生物種群結(jié)構(gòu),減少系統(tǒng)中以 N2O 作為最終產(chǎn)物的菌群數(shù)量也可實(shí)現(xiàn) N2O 的減量化。目前,類似研究在實(shí)際工程中的應(yīng)用并不多見。在全球日趨變暖的大形勢(shì)下,如何將污水處理中釋放的 N2O 減量是今后研究的一個(gè)主要方向,也是對(duì)科研工作者提出的一大挑戰(zhàn)。
參考文獻(xiàn):
[1] 石明巖,呂錫武,稻森悠平.N2O 的環(huán)境效應(yīng)及其防治技術(shù)的發(fā)展趨勢(shì)[J].城市環(huán)境與城市生態(tài),2002,15(5):45-47.
[2] Sharma C, Gupta P K, Parashar D C.Atmospheric nitrous oxide: sources and sinks [J]. Tropical Ecology, 1996, 37(2):153-166.
[3] 高素華,潘亞茹.溫室效應(yīng)對(duì)氣候和農(nóng)業(yè)的影響[J].環(huán)境科學(xué),
1991, 12(2):73-76.
[4] 劉秀紅,彭永臻,馬濤,尚會(huì)來(lái),吳昌永.硝化類型對(duì)污水脫氮過程中N2O 產(chǎn)生量的影響[J].中國(guó)環(huán)境科學(xué),2007,27(5):633-637.
[5] 尚會(huì)來(lái),彭永臻,王淑瑩,等.污水生物脫氮過程中N2O 的產(chǎn)生和減量化控制[J].中國(guó)給水排水,2008,24(16):104-108.
[6] M D Butler, Y Y Wang, E Cartmell, et al. Nitrous oxide emissions for early warning of biological nitrification failure in activated sludge [J].Water Research, 2009, 43(5), 1265-1272.
[7] Van Niel E W J, Arts P A M, Wesselink B J, et al. Competition between heterotrophic and autotrophic nitrifiers for ammonia in chemostat cultures [J].FEMS Microbiology Ecology,1993,102 (2), 109-118.
[8] Anderson I C, Poth M, Homstead J, et al. A comparison of nitric oxide and nitrous oxide production by the autotrophic nitrifier Ni- trosomonas europaea and the heterotrophic nitrifier Alcaligenes faecalis [J]. Applied and Environmental Microbiology, 1993, 59 (11), 3525-3533.
[9] Inamori Yuhei,Wu Xiao-Lei,Mizaochi Motoyuki.N2O producing capability of nitrosomonas europaea,nitrobacter winograski and alcaligenes faecalis [J].Water Science and Technology,1997,36 (10):65-72.
[10] 劉秀紅,楊慶,吳昌永,等.不同污水生物脫氮工藝中 N2O 釋放量及影響因素[J].環(huán)境科學(xué)學(xué)報(bào),2006,26(12):1940-1947.
[11] Gaelle Tallec, Josette Garnier, Gilles Billen, et al. Nitrous oxide e- missions from denitrifying activated sludge of urban wastewater treatment plants, under anoxia and low oxygenation [J].Biore- source Technology,2008,99(7):2200-2209.
[12] Asma Alinsafi, Nouceiba Adouani, Fabrice Beline, et al. Nitrite effect on nitrous oxide emission from denitrifying activated sludge [J]. Process Biochemistry, 2008(43):683-689.
[13] Hanaki K, Hong Z, Matsuo T. Production of nitrous oxide gas during denitrification of wastewater [J]. Water Science and Tech- nology, 1992, 26(5-6):1027-1036.
[14] Bonin P, Gilewicz M, Bertrand J C. Effect of oxygen on each step of denitrification on Pseudomonas nautica [J]. Canadian Journal of Microbiology, 1989, 35(11), 1061-1064.
[15] Bleakley B H, Bruce H, Tiedje J M. Nitrous oxide production by organisms other than nitrfiers or denitrfiers [J].Applied and Envi- ronmental Microbiology, 1982, 44 (6), 1342-1348.
[16] 劉秀紅,彭軼,馬濤,等. DO 濃度對(duì)生活污水硝化過程中 N2O 產(chǎn)生量的影響[J].環(huán)境科學(xué),2008,29(3):660-664.
[17] Galle Tallec, Josette Garnier, GillesBillen, et al. Nitrous oxide e- missions from secondary activated sludge in nitrifying conditions of urban wastewater treatment plants: effect of oxygenation level [J].Water Research, 2006, 40(15):2972 - 2980.
[18] 趙宗升,劉鴻亮,李炳偉,等.高濃度氨氮廢水的高效生物脫氮途徑[J].中國(guó)給水排水,2001,17(5):24-28.
[19] Sunjin Hwang, Kwangun Jang, et al. Factors affecting nitrous ox- ide production: a comparison of biological nitrogen removal pro- cesses with partial and complete nitrification [J].Biodegradation,
2006, 17(1):19-29.
[20] Hiroki Itokawa, Keisuke Hanaki, Tomonori Matsuo. Nitrous ox- ide production in high-loading biological nitrogen removal pro- cess under low COD/N ratio condition [J]. Water Research, 2001, 35(3), 657-664.
[21] Marlies J Kampschreur, et al. Dynamics of nitric oxide and nitrous oxide emission during full-scale reject water treatment [J]. Water Research, 2008, 42(3):812-826.
[22] Lemaire R, Meyer R, Taske A, et al. Identifying causes for N2O accumulation in a lab-scale sequencing batch reactor performing simultaneous nitrification, denitrification and phosphorus removal [J]. Journal of Biotechnology, 2006, 122(1):62-72.
[23] Yan Zhou, Maite Pijuan, Raymond J, et al. Free nitrous acid inhi- bition on nitrous oxide Reduction by a denitrifying-enhanced bio- logical phosphorus removal sludge [J].Environmental Science & Technology,2008,42(22),8260-8265.
[24] 蔣勝韜,王三秀,萬(wàn)金保.同步硝化反硝化研究進(jìn)展[J].江西科學(xué),2008,26(6):905-909.
[25] Zeng R J ,van Loosdrecht M C M,Yuan Z G, et al. Metabolic model for glycogen accumulating organisms in anaerobic/ aerobic activated sludge systems[J]. Biotechnology and Bioengineering, 2003, 81(1):92-105.
[26] F Beline, J Martinez, C.Marol, et al. Application of the 15N tech- nique to determine the contributions of nitrification and denitrifi- cation to the flux of nitrous oxide from aerated pig slurry[J].Water Research,35(11):2774-2778.
[27] 呂錫武,稻森悠平,等.同步硝化反硝化脫氮及處理過程中 N2O的控制研究[J].東南大學(xué)學(xué)報(bào),2001,31(1):95-99.
[28] 阮文權(quán),陳堅(jiān).好氧顆粒污泥同步硝化反硝化脫氮過程中 N2O的產(chǎn)生[J].無(wú)錫輕工大學(xué)學(xué)報(bào), 2004,23(4) :37-40.
[29] Voets J P. Removal of nitrogen from highly nitrogenous wastewater [J].Journal Water Pollution Control Federation,1975,47(2):394-398.
[30] Kartal B, Kuypers M M M, Lavik G Schalk J, et al. Anammox bacteria disguised as denitrfiers: nitrate reduction to dinitrogen gas via nitrite and ammonium [J].Environmental Microbiology, 2007, 9(3), 635-642.
[31] 陳旭良.短程硝化- 厭氧氨氧化工藝處理味精廢水的研究[D].杭州:浙江大學(xué),2006.
[32] Zeng R J, Yuan Z, K eller J, et al. Enrichment of denitrifying glycogen accumulating organisms in anaerobic/anoxic activated sludge system [J].Biotechnology and Bioengineering,2003,81(4) : 397-404.
[33] Romain Lemaire, et al. Identifying causes for N2O accumulation in a lab-scale sequencing batch reactor performing simultaneous
nitrification, denitrification and phosphorus removal[J].Journal of Biotechnology,2006,122(1):62-72.
[34] Hippen A, Baumgarten G, Rosenwinkel K-H, et al. F.Aerobic
deammonification-A new experience in the treatment of wastewa- ter. Water Science and Technology, 1997, 35(10):111-120.
[35] Muller E B, et al. Simultaneous NH3 oxidation and N2 production at reduced O2 tensions by sewage sludge subcultured with chemolithotrophic medium [J].Biodegradation,1995,6(4):339-349.
蘇州湛清環(huán)保科技有限公司
熱線:400-110-8500
傳真:0512-50310052
郵箱:sales@drtsing.com
地址:江蘇省蘇州市昆山玉帶西路樂邦產(chǎn)業(yè)園